Männer erkranken schwerer, Frauen leiden länger…
Die Corona-Pandemie hat es wieder gezeigt: das vermeintlich „starke Geschlecht“ hat nach einer Infektion mit dem SARS-Cov-2-Virus einen deutlich schlechteren klinischen Verlauf, die Sterblichkeitsrate ist für Männer sogar höher als für Frauen. Sind Männer also in Wirklichkeit das „schwächere Geschlecht“? Ist der „Männerschnupfen“ doch wirklich schlimmer, ist das Lästern über die männliche Wehleidigkeit also unbegründet? Die Corona-Pandemie zeigte aber auch, dass Frauen an den Folgen der Corona-Infektion, dem „Long-Covid-Syndrom“ deutlich stärker leiden als Männer.
Sind es „nur“ die Hormone oder noch andere Faktoren, die Frauen von Männern unterscheidet?
In der Tat scheint die geschlechtsspezifische Verteilung von Hormonen eine wichtige Rolle zu spielen, wie zahlreiche Studien belegen: Östrogene würden demnach die Immunabwehr stärken, Testosteron sie dagegen schwächen. Testosteron fördert die stärkere Risikobereitschaft des Mannes, auch im Krankheitsfall: häufig übt der Mann auch dann die Rolle des „Jägers und Sammlers“ aus, achtet weniger auf sich und gefährdet damit die Genesung. Ein hoher Testosteronspiegel erhöht auch das Risiko für Herzkrankheiten. Männer sind zudem von vielen Krebserkrankungen häufiger betroffen. Das Risiko, an einer bösartigen Krankheit zu sterben, ist bei ihnen oft höher als bei Frauen. Bei Typ-2-Diabetes entfaltet Östrogen eine gewisse Schutzwirkung. Dies erklärt, warum das Risiko für diese Stoffwechselkrankheit bei Frauen nach den Wechseljahren, wenn der Östrogenspiegel sinkt, ansteigt (PZ30.07.2020).
Risikofaktor für Autoimmunerkrankungen: Geschlecht „weiblich“, das doppelt „X“
Schilddrüsenerkrankungen, Multiple Sklerose, Rheumatoide Arthritis oder Lupus erythematodes: Frauen sind am häufigsten betroffen, 78% der Betroffenen sind weiblich (Spectrum 21.2.2022).
Gerade Schilddrüsenerkrankungen treten bei Frauen viel häufiger auf als bei Männern. Im Vergleich zu Männern haben Frauen ein 3-4 mal höheres Risiko für gutartige und bösartige Schilddrüsenerkrankungen. Schilddrüsenüberfunktionen werden bei Frauen im Vergleich zu Männern bis zu 10-mal häufiger beobachtet. Die Häufigkeit von Hyperthyreosen („Überfunktion“) wird mit circa 2 % bei Frauen und 0,2 % bei Männern geschätzt. Die häufigste Ursache einer Schilddrüsenüberfunktion ist der Morbus Basedow (60–80 %), der deutlich häufiger bei Frauen als bei Männern auftritt (5 : 1 bis 10 : 1).
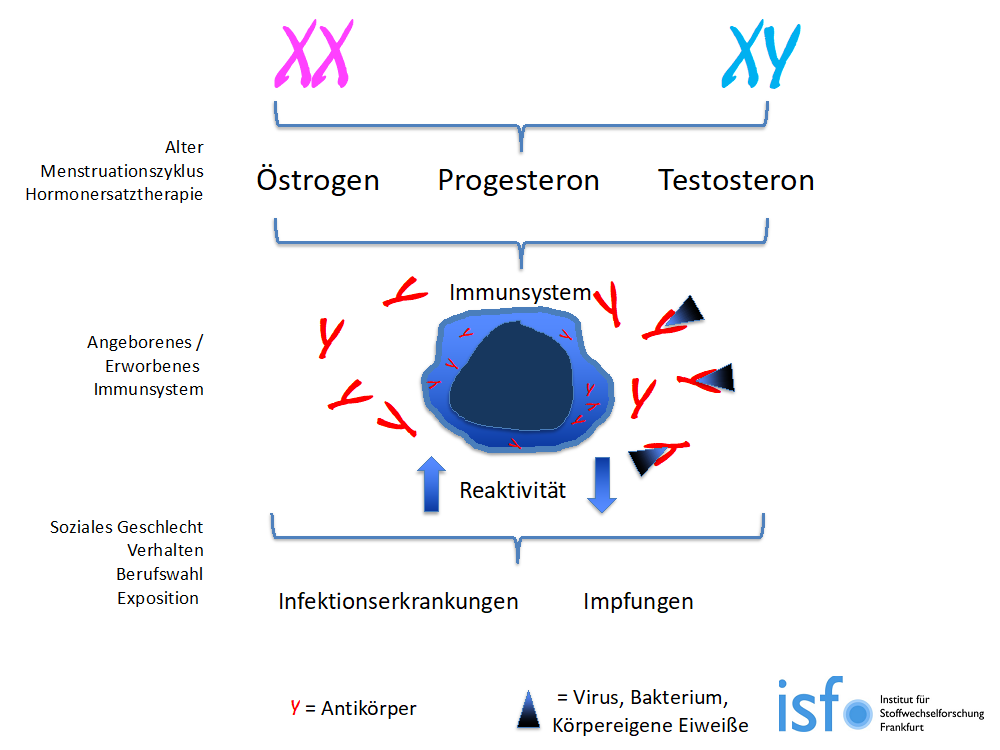
Abbildung 1
Geschlechtsspezifische Einflussfaktoren auf das Immunsystem
Die Sexualhormone beeinflussen über spezifische Rezeptoren auf den Immunzellen (z.B. Antikörper produzierende Lymphozyten) das Immunsystem, zum einen stimulierend (Östrogene), zum anderen hemmend (Testosteron). Die Sexualhormone unterliegen Schwankungen durch Alter, den Menstruationszyklus oder eine Hormonersatztherapie. Genetische, anatomische und hormonelle Faktoren beeinflussen unser angeborenes und erworbenes Immunsystem und dessen Reaktivität auf Infektionskrankheiten und Impfungen. Zudem bestehen weitere Einflussfaktoren wie das soziale Geschlecht (= Erwartung des Umfelds an „Frau“ oder „Mann“) mit Konsequenzen auf Verhalten, Berufswahl und Exposition gegenüber Krankheitserregern oder körpereigenen Zellbestandteilen (Eiweiß). Werden diese körpereigenen Zellbestandteile vom eigenen Immunsystem angegriffen, spricht man von Autoimmunerkrankungen.
Die weitaus häufigste Ursache für eine Schilddrüsenunterfunktion ist die Autoimmunthyreoiditis (Hashimoto-Thyreoiditis). Bei dieser Erkrankung kommt es zu einer Infiltration der Schilddrüse durch Lymphozyten (dienen eigentlich der Abwehr von Viren und beginnenden Fehlsteuerungen in der Zelle), die das Organ langfristig schädigen können. Dieser Angriff des körpereigenen Immunsystems (= Autoimmunerkrankung) kann die Funktion der Schilddrüse beeinträchtigen. Die Erkrankung ist häufig durch einen langjährigen chronischen Verlauf gekennzeichnet. Die Therapie besteht häufig in der Gabe von Schilddrüsenhormonen, da die Hormonproduktion abnimmt. Es gibt aber auch symptomlose Verläufe, ohne dass sich die Schilddrüsenfunktion im Laufe der Jahre ändert. Bereits früh sind typische Ultraschallveränderungen sowie erhöhte Autoantikörper (TPO-Antikörper) nachweisbar. Auffällig ist das gehäufte Auftreten bei Frauen, die bis zu 10-mal häufiger als Männer betroffen sind, sowie das mit dem Lebensalter steigende Risiko für diese Autoimmunerkrankung.
Eine Rolle dabei scheint das Östrogen zu spielen. In einer Übersichtsarbeit von Michael Derwahl und seiner Kollegin Diana Nicula steigt die Inzidenz von malignen Schilddrüsenerkrankungen bei Frauen von der Pubertät bis zur Menopause im Vergleich zu Männern bis zum 14- fachen. Mit anderen Worten: mit Beginn der Pubertät haben Frauen ein deutliches erhöhtes Risiko für Schilddrüsentumore. In der Menopause aber, wenn also Östrogen nicht mehr ausreichend vorhanden ist, gleicht sich das Risiko bei Mann und Frau an (Endocrine Related cancer 2014,21: T273). Es gibt mehrere Erklärungen für dieses erhöhte Risiko: das weibliche Hormon Östrogen gilt als ein starker Wachstumsfaktor und stimuliert Schilddrüsenzellen. Vor allem beim papillären Schilddrüsenkarzinom ist Östrogen ein starker Vermittler für diese Fehlregulation in der Schilddrüse. Ferner reguliert das Östrogen auch die Gefäßneubildung, die bei einer Krebserkrankung die Metastasierung fördert (Ärzte Zeitung 11.3.2022).
In der Corona - Pandemie waren Frauen stärker betroffen von der Folge dieser Virusinfektion als Männer. Vermutet werden eine starke Autoimmunreaktion und psychosoziale Belastungen, die die Schwere der Erkrankung bei Frauen beeinflussen. Wahrscheinlich liegt es an dem X - Chromosom: viele für das Immunsystem bedeutende Gene liegen ausschließlich auf dem X - Chromosom. Da Frauen bekanntlich zwei X - Chromosome haben, verfügen sie über ein sehr stark ausgeprägtes Immunsystem. Im Chromosom, das sich im Zellkeren jeder Zelle befindet, ist der gesamte „Bauplan“, unsere Erbsubstanz, in Form von „Genen“ gespeichert. In der Zelle programmieren diese Gene die Merkmale der jeweiligen Zelle, also z.B. der Muskelzelle oder der Schilddrüsenzelle.
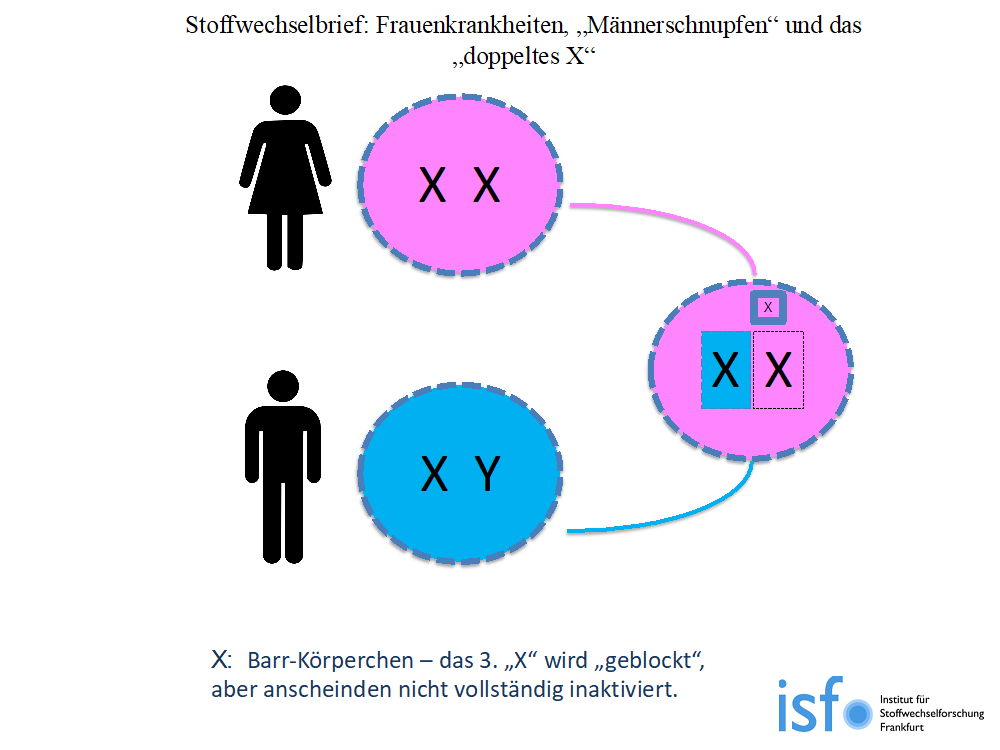
Abbildung 2
Das 2. „X-Chromosom“ wird inaktiviert.
Da ein X-Chromosom von der Frau zu viel ist, wird dieses bereits in der Embryonalphase „inaktiviert“, man kennt dieses inaktivierte X-Chromosom als „Barr-Körperchen“. Bisher ging man davon aus, dass dieses stillgelegte X-Chromsom keine Bedeutung hat. Allerdings zeigt sich, dass von dieser „Gen-Masse“ (= X - Chromosom) bis 15 % der Gene doch aktiv sind, d.h. diese Erbfaktoren beeinflussen zusätzlich das Immunsystem. Bei bestimmten Erkrankungen korreliert der Schwergrad der Erkrankung mit der Anzahl der Gene auf beiden X-Kopien. Dies mag erklären, warum Frauen ein deutlich vielfältigeres Spektrum an Abwehrmechanismen haben und deshalb vermehrt an Autoimmunerkrankungen leiden, wie Hashimoto, Morbus Basedow (Schilddrüsenerkrankungen, Rheuma), aber auch Long COVID (= Beginn der Infektion bis weitere Beschwerden lange nach der Infektion): bei Organveränderungen sowie nach Infektionen kann diese überschießende Abwehrreaktion des weiblichen Immunsystem körpereigene Zellen angreifen und zerstören (Autoimmun = „Selbstabwehr“). Zudem hat das Hormon Östrogen einen stark immunmodulierenden Effekt. Die virale Infektabwehr ist bei Frauen deutlich aktiver, dies zeigt sich in höheren Immunglobulinen (= Antikörper = Eiweiße, die Erreger und Tumorzellen unschädlich machen, Abbildung 1) und höheren zirkulierenden – T Zellen verglichen mit Männern.
Auffallend in der Corona Pandemie war, dass die psychosoziale Belastung bei Frauen einen deutlichen Einfluss hat auf das Long – Covid-Syndrom. Hier zeigen sich Parallelen zum „Chronic Fatigue-Syndrome“, das häufig durch eine hohe Stressbelastung ausgelöst wird und oft Folge einer posttraumatischen Belastungsstörung ist. Unter Stress wird vermehrt und vor allem dauerhaft Cortisol ausgeschüttet. Kurzfristig erhöht Cortisol unter Stressbelastung die Abwehrbereitschaft, langfristig aber verringert es die Immunantwort auf zellulärer Ebene: das erklärt auch, warum wir häufig zu Beginn des Urlaubs, wenn wir eine stressige berufliche Phase hinter uns haben, krank werden. In der Behandlung zahlreicher Erkrankungen nutzt man diese Wirkung des Cortisons: durch hohe Cortisongaben werden die Abwehrzellen dauerhaft in ihrer Funktion unterdrückt werden. Der genaue Mechanismus ist allerdings noch unklar (Akt.Rheumatol.2021,46,258-266).
Sind Frauen hohen Belastungen ausgesetzt, schwächt der dauerhaft hohe Cortisonspiegel das Immunsystem. Viren haben es dann leichter, ihre Erbinfektion in die Zellen des weiblichen Organismus einzuschleusen (= Infektion). Erkennt dann das Immunsystem diese virusbedingte „Umprogrammierung“ im weiblichen Organismus, findet anscheinend eine massive Immunreaktion statt, vielleicht eine „Überreaktion“ – so die Hypothese.
Umgekehrt deutet sich an, dass Frauen besser auf Grippeimpfungen mit einer stärkeren Immunantwort reagieren und durch diese besser geschützt werden als Männer. Außerdem fiel auf, dass die Immunreaktion auf die Impfung umso schwächer ausfiel, je höher der männliche Testosteronspiegel war: je höher der Testosteronspiegel, desto stärker der Männerschnupfen?
Auch wenn die durch Östrogen vermittelte stark Immunreaktion Nachteile mit sich zieht, überwiegen dennoch die Vorteile: zahlreiche Tumore oder Krebsformen werden durch dieses spezialisierte Immunsystem unterdrückt, Herzkreislauferkrankungen treten vor der Menopause nur sehr selten auf. Ein weiteres Hormon, das für die Regulation des weiblichen Zyklus elementar ist, ist das Progesteron. Es entfaltet zusätzliche Wirkungen, die den weiblichen Körper vor zahlreichen Gefahren und Veränderungen schützen, vor allem zu Beginn und während der Schwangerschaft.
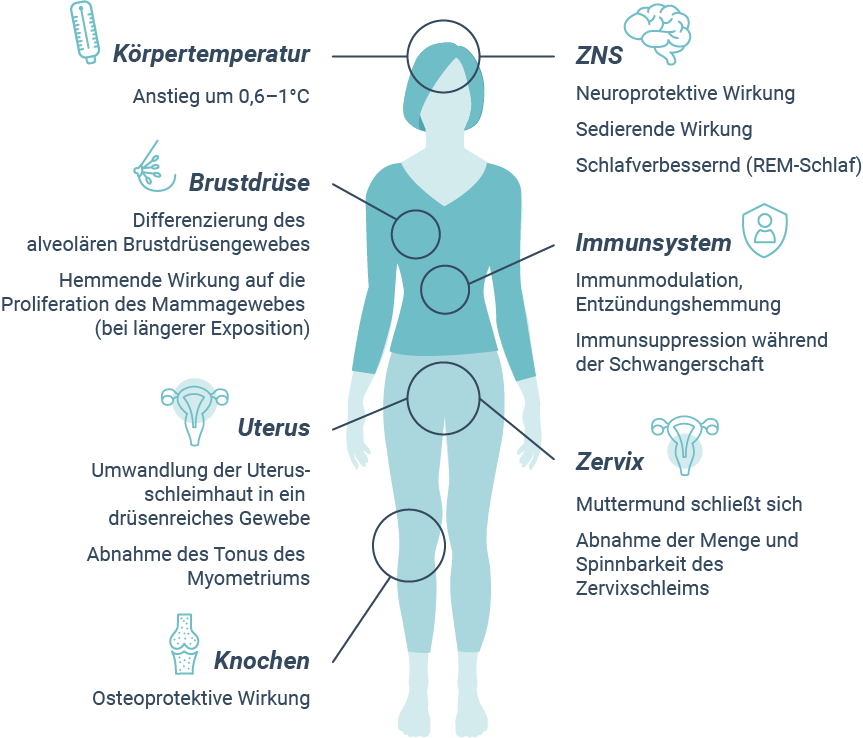
Abbildung 3
Progesteron hat beruhigende Wirkungen auf die Psyche, wirkt entzündungshemmend und ist wichtig für die Schwangerschaft (https://www.hormonspezialisten.de)
Toleranz und Schwangerschaft
Offensichtlich ist die Entwicklung von Autoimmunerkrankungen bei gebärfähigen Frauen der Preis dafür, dass eine Schwangerschaft überhaupt möglich ist: das Immunsystem der Frau muss ein fremdes Eiweiß, eine befruchtete Eizelle, mit genetischen und immunologischen Informationen des Mannes annehmen, das Einnisten in die Gebärmutter erlauben und über 9 Monate auch tolerieren. Normalerweise müsste der Körper der Frau auf diese Befruchtung mit einer massiven Abwehrreaktion antworten, denn es sind ja „fremde“ Zellen.
Die Evolutionsbiologin Melissa Wilson nannte diese Fähigkeit des weiblichen Immunsystems „Schwangerschaftskompensation“: die Plazenta oder „Mutterkuchen“, die den Fötus mit Sauerstoff und Nährstoffen versorgt, muss in die Gebärmutter der Frau „einwachsen“. Während der Schwangerschaft muss der weibliche Organismus den wachsenden Fötus, dessen Erbinformation zur Hälfte vom Vater stammt und damit fremd ist, tolerieren.
Wie Wilson vermutet, hat sich der weibliche Organismus auf die vorübergehenden immunologischen Herausforderungen eingestellt. Zu Beginn der Schwangerschaft nehmen bestimmte Immunreaktionen zu, was der Plazenta hilft, neue Blutgefäße zu bilden. Ab der Mitte der Schwangerschaft lassen Immunität und Entzündungsreaktion nach, um sich dann in Vorbereitung zur Geburt hin wieder zu verstärken. Die Autoimmunität könnte ein unerwünschter Nebeneffekt der komplexen Immunprozesse sein, auf die der weibliche Organismus angewiesen ist, um Kinder auf die Welt zu bringen.
In der Schwangerschaft blockiert Progesteron zahlreiche immunologische Reaktionen, was erklärt, warum in der Schwangerschaft Immunerkrankungen wie z.B. Multiple Sklerose oder Rheumatoide Arthritis eine geringere Symptomatik entfalten. Nach der Entbindung fallen die Hormone dramatisch ab und können dann einen erneuten Krankheitsschub auslösen. Doch trotz ihrer offenbar wichtigen Rolle können Sexualhormone nicht alles erklären. Denn manche Leiden, wie Lupus erythematodes oder Multiple Sklerose, brechen mitunter bereits in der Kindheit aus – also bevor die Spiegel von Östrogen und Progesteron in der Pubertät ansteigen. Es müssen demnach weitere Faktoren beteiligt sein.
Mehr Schwangerschaften – weniger Autoimmunerkrankung? Vor 50 Jahren bekamen Frauen mehr Kinder als heute. In der Tat: in dieser Zeit waren Autoimmunerkrankungen bei Frauen deutlich geringer. Aber auch die Umwelt spielt eine Rolle: bei eineiigen Zwillingen kann ein Zwilling auch eine Autoimmunerkrankung bekommen, während der andere praktisch gesund bleibt. Einige Forscher konzentrieren sich daher auf den augenfälligsten zellulären Unterschied zwischen Mann und Frau: das zweite X-Chromosom.
Herzschmerz - Frauen leiden anders
„Schmerzen in der linken Brustseite, Ausstrahlen bis in den Hals“ – die typischen Herzinfarkt - Symptome, wir kennen sie alle. Dies trifft aber nicht bei Frauen zu. Ursache: die Symptomatik für Herz-Kreislauf-Erkrankungen wurden in den letzten Jahrzehnten überwiegend an Männern untersucht und weniger an Frauen. Frauen leiden anders! Soziokulturelle Unterschiede, die Interaktion der Frau mit ihrer Umwelt und Gesellschaft wie auch ein anderer Lebensstil definieren das Risiko für Herz-Kreislauf-Erkrankungen bei Frauen. Hohe Belastungen werden von Frauen, dank Östrogen und Progesteron, ganz anders wahrgenommen und verarbeitet. Beide Hormone scheinen sogar die Frauen vor Herzkreislauferkrankungen zu schützen Die Frau erleidet beispielsweise einen Herzinfarkt durchschnittlich erst neun Jahre später als der Mann. In der Postmenopause erreicht die Frau jedoch die Inzidenzrate des Mannes.
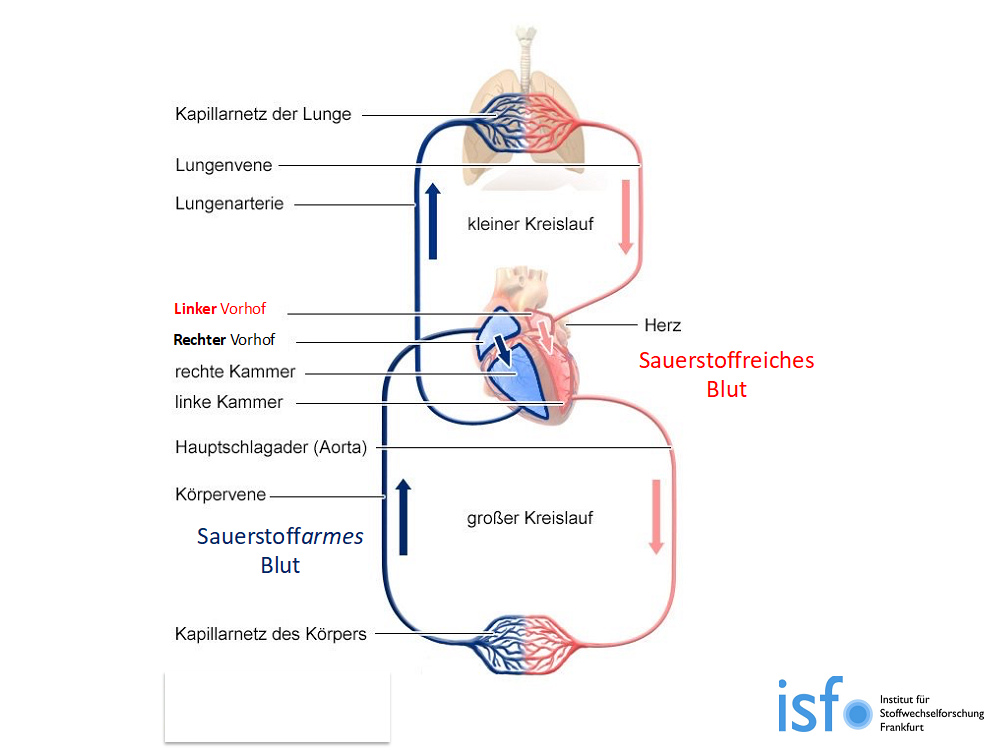
Abbildung 4
Das Herz besteht aus zwei Hälften, dem rechten und dem linken Herz. Das rechte Herz funktioniert wie eine Ansaugpumpe: das sauerstoffarme Blut wird aus den Beinen, dem Bauch und dem Kopf angesaugt und wird dann in die Lunge weitergeleitet. In der Lunge („Kapillarnetz“) wird das sauerstoffarme Blut mit Sauerstoff angereichert und weitergeleitet in den linken Vorhof. Im linken Vorhof wird das Blut in Portionen in die linke Kammer weitergeleitet, dann wird es über die große Hauptschlagader in den gesamten Körper gepumpt. Das Pumpen des Herzens, auch Systole (1. Blutdruckwert) genannt, können wir tasten: es ist unser Puls. Das linke Herz ist entscheidend für die Sauerstoffversorgung des gesamten Körpers. In der Ruhephase füllt sich das Herz (Vorhöfe und Kammern, Diastole genannt).
Die Hormonersatztherapie in der Frühphase der Menopause schützt Frauen vor Herzkreislauferkrankungen, allerdings lässt diese Wirkung im Laufe der Menopause nach. Die Mechanismen sind nicht geklärt (Cancer J. 2022 ; 28(3): 208–223) .
Wenn wir älter werden, ändert sich auch unsere Herzleistung. Bei Frauen ändert sich diese Herzleistung allerdings langsamer als bei Männern. Eine Einschränkung der Herzleistung nennt man „Herzinsuffizienz“ oder Herzmuskelschwäche. Die Hauptursache bei Männern für diese Herzmuskelschwäche ist eine Verkalkung der Herzkranzgefäße und eine daraus resultierende verringerte Durchblutung der Herzmuskelzellen. Der Herzinfarkt, der akute Verschluss eines Herzkranzgefäßes, stoppt den Blutfluss an dem betreffenden Herzmuskel, das Gewebe stirbt ab, die Pumpleistung wird geringer.

Abbildung 5
Ein Herzinfakt bei Frauen verursacht häufig keine typischen Beschwerden in der der Herzgegend
Bei Frauen ist dies völlig anders: wenn Frauen älter werden, entspannen sich der Vorhof und die Kammer schlechter („diastolische Dysfunktion“), der „unentspannte“ Herzmuskel steht unter einem hohen „Dauerdruck“, er nimmt sogar an Dicke zu. Die Herzleistung bleibt aber lange Zeit erhalten. Durchblutungsstörungen wie beim Mann infolge einer Verkalkung treten seltener auf. Die Durchblutungsstörungen beim weiblichen Herzmuskel sind in der Regel eine akute Verengung der Herzkranzgefäße infolge von Stress („Gefäßkrampf“) oder ein Verschluss von ganz kleinen Arterien im Herzmuskel.
Auffällig ist, dass klassische Risikofaktoren unterschiedliche Auswirkungen bei Frauen und Männer haben. So ist Rauchen bei Frauen mit einem höheren Risiko für Herzerkrankungen verbunden als bei Männern. Bluthochdruck führt bei Frauen häufiger zu Herzinfarkt als bei Männern, Diabetes mellitus verursacht bei Frauen stärker eine Durchblutungsstörung der Herzkranzgefäße als bei Männern. Schon erhöhte Nüchternzuckerspiegel oder ein erhöhter Langzeitzuckerwert (HbA1c) erhöhen das Risiko bei Frauen für Durchblutungsstörungen des Herzmuskels stärker als bei Männern. Auch frauenspezifische biologische kardiovaskuläre Risikofaktoren wie Schwangerschaftsbluthochdruck, Schwangerschaftsdiabetes, vorzeitige Entbindung und frühe Menopause erhöhen das Herzkreislauferkrankungsrisiko.
Während die postmenopausale Frau in den westlichen Gesellschaften häufiger eine Herzmuskelschwäche (Herzinsuffizienz) mit erhaltener normaler Auswurfleistung und diastolischer Dysfunktion hat (HFpEF), entwickelt der Mann gleichen Alters eine Herzmuskelschwäche mit eingeschränkter linksventrikulärer systolischer Funktion. Männer haben deshalb eine andere Symptomatik: nimmt die Herzleistung ab, staut sich das Blut in der Lunge, der Patient hat dann Wasser in der Lunge, es „brodelt“. Frauen verspüren die veränderte Herzleistung erst viel später. Durch den langsamen Verlauf wird das Herzmuskelgewebe aber stärker geschädigt, das geringe Beschwerdebild verhindert eine frühzeitige Therapie.
Nicht vergessen:
Reanimation: immer „Drücken“
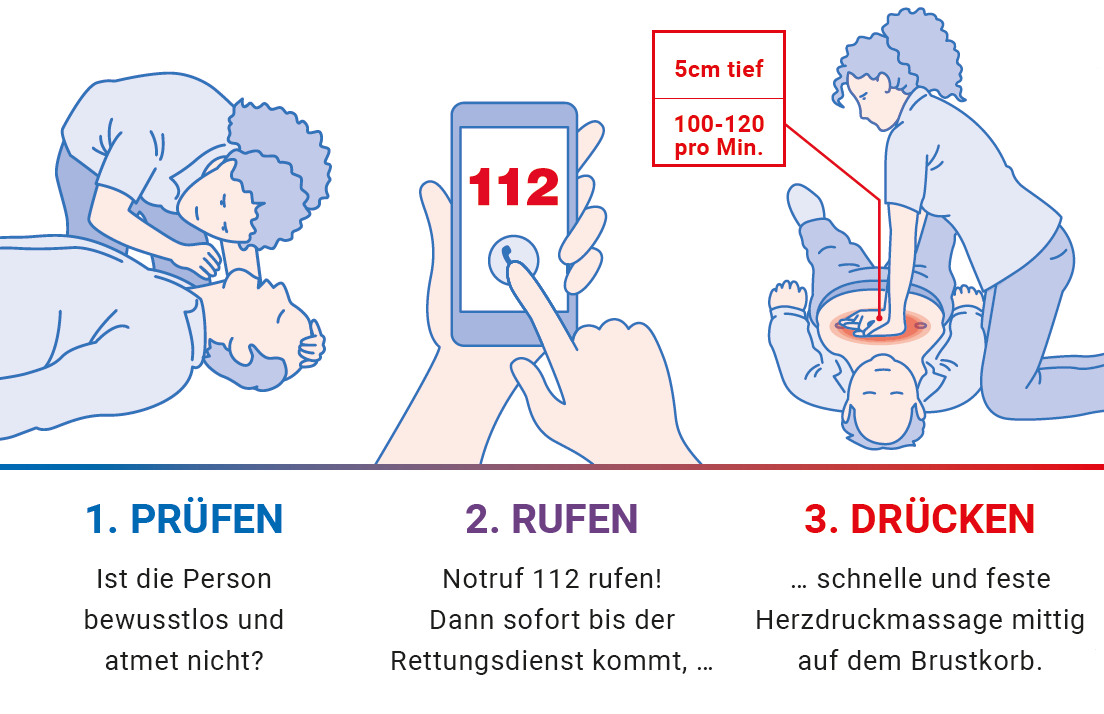
Abbildung 6
Schema der Laienreanimation: "Prüfen, Rufen, Drücken", BZgA


